Скільки електронних орбіталей має атом літію: детальний огляд для всіх рівнів
Атом літію, цей скромний елемент з атомним номером 3, ховає в собі цілий всесвіт квантових таємниць, які розкривають, як працює матерія на найглибшому рівні. Його електронна структура нагадує просту, але елегантну будівлю, де кожен “поверх” визначає, як елемент взаємодіє зі світом. Розбираючись у кількості електронних орбіталей літію, ми не просто рахуємо абстрактні одиниці – ми занурюємося в основи хімії, які пояснюють, чому літій такий реактивний і корисний у сучасних технологіях, від батарей до ліків.
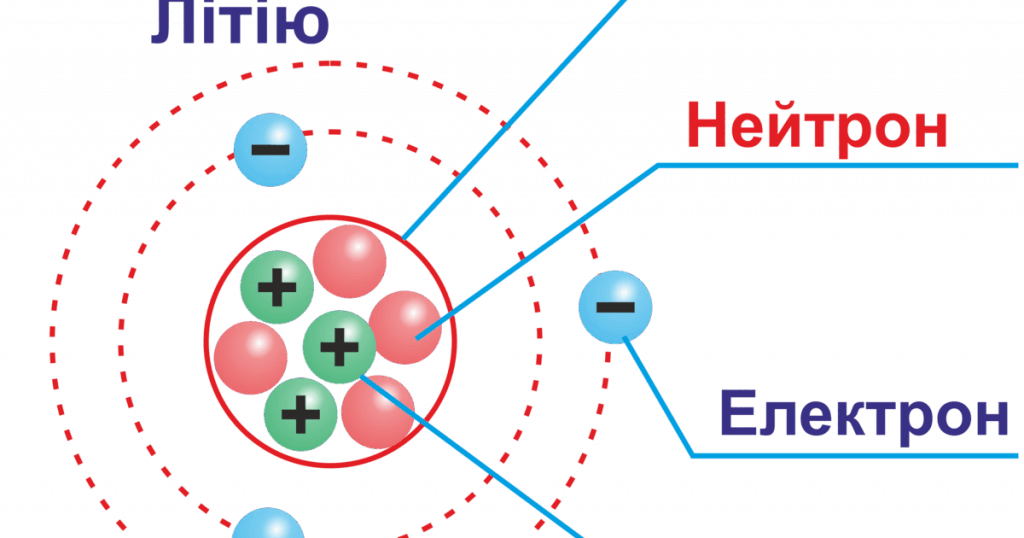
Літій стоїть на початку періодичної таблиці, і його атом складається з ядра з трьома протонами та, зазвичай, чотирма нейтронами, оточеними трьома електронами. Ці електрони не просто кружляють довкола, як планети навколо сонця – вони існують у хмарах ймовірностей, відомих як орбіталі. Розуміння цього допомагає не тільки студентам, але й усім, хто цікавиться наукою, побачити красу в невидимому.
Що таке електронні орбіталі: основи для початківців
Електронні орбіталі – це не просто траєкторії, а радше області простору навколо атомного ядра, де ймовірність знайти електрон найвища. Уявіть орбіталь як туманну хмару, що пульсує енергією, де електрон може з’явитися в будь-якій точці, але з певною ймовірністю. Ця ідея походить від квантової механіки, де класичні уявлення про точні орбіти замінюються хвильовими функціями.
Для початківців важливо знати, що орбіталі класифікуються за квантовими числами: головним (n), яке визначає енергетичний рівень, орбітальним (l), що вказує на форму, магнітним (m_l) для орієнтації та спіновим (m_s) для напрямку спіна електрона. Наприклад, на першому рівні (n=1) є лише s-орбіталь, куляста і симетрична, ніби ідеальна сфера, що обіймає ядро.
Переходячи до складнішого, орбіталі заповнюються за правилом Гунда та принципом Паулі, де кожна орбіталь може вмістити до двох електронів з протилежними спінами. Це створює стабільність, подібну до пари танцюристів, які рухаються в гармонії, не стикаючись. Без цього розуміння важко уявити, чому атоми поводяться саме так, а не інакше.
Будова атома літію: крок за кроком
Атом літію має електронну конфігурацію 1s² 2s¹, що означає два електрони на першому рівні та один на другому. Ядро, з трьома протонами, притягує ці електрони з силою, яка зменшується з відстанню, роблячи зовнішній електрон вразливим до реакцій. Ця структура робить літій лужним металом, готовим віддати свій валентний електрон, ніби щедрий дарувальник у хімічному світі.
Детальніше: на рівні n=1 є одна s-орбіталь, заповнена двома електронами. На рівні n=2 – ще одна s-орбіталь з одним електроном. Таким чином, загальна кількість орбіталей в атомі літію дорівнює двом. Але чому не більше? Бо літій має лише три електрони, і вони займають найнижчі доступні енергетичні стани, слідуючи принципу мінімальної енергії.
Для просунутих читачів цікаво відзначити, що в багатоелектронних атомах, як літій, орбіталі не ідеально водневоподібні через екранування – внутрішні електрони послаблюють притягання ядра для зовнішнього. Це призводить до того, що енергія 2s-орбіталі в літії нижча, ніж у водні, роблячи атом стабільнішим, але реактивним.
Квантові числа в дії для літію
Розгляньмо квантові числа для електронів літію. Перші два електрони на 1s-орбіталі мають n=1, l=0, m_l=0, з m_s +1/2 і -1/2. Третій електрон: n=2, l=0, m_l=0, m_s +1/2. Це точний опис, який дозволяє передбачити спектральні лінії чи магнітні властивості.
Якщо ви початківець, подумайте про це як про адресу в багатоквартирному будинку: n – поверх, l – тип квартири, m_l – номер, m_s – напрямок ключа. Літій займає лише дві “квартири”, але вони визначають усе – від плавлення при 180°C до використання в термоядерних реакторах.
Скільки саме орбіталей: точний розрахунок
Отже, скільки електронних орбіталей має атом літію? Відповідь – дві: одна 1s і одна 2s. Це не випадково; кількість орбіталей на рівні визначається формулою 2l+1, але для s-орбіталей (l=0) це завжди одна. З трьома електронами літій не заповнює p-орбіталі (l=1), які з’являються на рівні n=2 з трьома орбіталями.
Порівняймо з сусідами: берилій (атомний номер 4) має ту ж конфігурацію, але з 2s², все ще дві орбіталі. Бор (5) додає 2p¹, збільшуючи до трьох. Літій – мінімаліст, і ця простота робить його ідеальним для вивчення базових принципів.
Для просунутих: у релятивістській квантовій механіці орбіталі літію описуються рівнянням Дірака, але для більшості цілей вистачає рівняння Шредінгера. Експерименти, як спектроскопія, підтверджують цю модель, показуючи енергетичні переходи точно між цими орбіталями.
Порівняння з іншими елементами
Щоб краще зрозуміти, ось таблиця порівняння кількості орбіталей для перших елементів.
| Елемент | Атомний номер | Конфігурація | Кількість орбіталей |
|---|---|---|---|
| Водень | 1 | 1s¹ | 1 |
| Гелій | 2 | 1s² | 1 |
| Літій | 3 | 1s² 2s¹ | 2 |
| Берилій | 4 | 1s² 2s² | 2 |
| Бор | 5 | 1s² 2s² 2p¹ | 3 (1s, 2s, одна 2p) |
Ця таблиця ілюструє, як з ростом атомного номера додаються орбіталі, заповнюючи оболонки. Дані базуються на стандартних моделях квантової хімії, підтверджених експериментами (за даними сайту uk.wikipedia.org та підручників з хімії).
Після вивчення таблиці стає ясно, чому літій унікальний: його неповна зовнішня орбіталь робить його високо реактивним, на відміну від стабільного гелію з повною 1s.
Застосування знань про орбіталі літію в реальному житті
Знання про орбіталі літію не абстрактне – воно лежить в основі літій-іонних акумуляторів, де іони літію переміщуються між електродами, використовуючи ту ж валентну 2s-орбіталь. Уявіть, як ваш смартфон працює завдяки цим двом орбіталям, що дозволяють літію легко втрачати електрон.
У медицині літій використовується для лікування біполярного розладу, впливаючи на нейрони через іонні канали, пов’язані з його електронною структурою. Для просунутих: дослідження 2025 року показують, що ізотопи літію, як ⁶Li, мають різні нейтронні захоплення, впливаючи на ядерні реакції в термоядерній енергетиці.
Початківцям раджу експеримент: візьміть шматок літію (обережно, він реактивний!) і киньте у воду – реакція демонструє, як зовнішня орбіталь віддає електрон, утворюючи гідроксид. Це живий приклад теорії в дії.
Глибші аспекти: гібридні орбіталі та квантові ефекти
Хоча атом літію має лише дві орбіталі, в сполуках як LiH виникають гібридні стани, де 2s змішується з p-орбіталями для утворення зв’язків. Це пояснює лінійну геометрію молекул, ніби орбіталі танцюють у парі, створюючи нові форми.
У квантовій хімії розрахунки методом Хартрi-Фока для літію показують, що енергія іонізації зовнішнього електрона становить близько 5.39 еВ, точно через структуру орбіталей. Просунуті читачі можуть зацікавитися багатоелектронними ефектами, де кореляція електронів додає нюанси до базової моделі.
Емоційно це захоплює: подумайте, як така проста структура пояснює, чому літій – ключ до зеленої енергії, допомагаючи боротися з кліматичними змінами через ефективні батареї.
Цікаві факти про орбіталі літію
- 🔬 Літій – найлегший метал, і його орбіталі роблять його щільністю меншою за воду, дозволяючи плавати – уявіть метал, що танцює на поверхні!
- 🌌 У зірках літій утворюється в перші хвилини після Великого Вибуху, з орбіталями, подібними до земних, але в екстремальних умовах.
- 🚀 NASA використовує літій у батареях для космічних місій, де стабільність орбіталей забезпечує надійність на мільйони кілометрів.
- 🧠 Дослідження 2025 року виявили, що квантові комп’ютери можуть симулювати орбіталі літію для моделювання складніших атомів, прискорюючи відкриття.
- ⚡ Літій має ізотоп ⁷Li, який у ядерних реакторах поглинає нейтрони, впливаючи на орбітальні переходи в плазмі.
Ці факти додають шарму до сухої теорії, показуючи, як орбіталі літію переплітаються з нашим життям. Від батарей електрокарів до зірок – все починається з цих двох простих орбіталей.
Типові помилки в розумінні орбіталей і як їх уникнути
Багато хто плутає орбіталі з орбітами Бора, думаючи, що електрони кружляють по колу. Насправді орбіталі – ймовірнісні, і в літії це особливо помітно через малий розмір. Інша помилка – ігнорування спіна, що призводить до неправильного заповнення.
Для уникнення: вивчайте діаграми, як на уроках хімії, і пам’ятайте, що в літії немає p-орбіталей у ґрунтовому стані. Просунуті можуть використовувати програмне забезпечення як Gaussian для візуалізації.
Ці поради роблять вивчення приємним, перетворюючи помилки на можливості для відкриттів.
Майбутнє досліджень орбіталей літію
У 2025 році вчені досліджують літій у квантових комп’ютерах, де орбіталі моделюють для створення нових матеріалів. Це може революціонізувати енергетику, роблячи батареї ефективнішими. Початківці, зацікавтеся: проста структура літію – ключ до складних інновацій.
Зрештою, розбираючись у цих орбіталях, ми бачимо, як мікросвіт формує макросвіт, від лабораторій до повсякденного життя.







