Йонний зв’язок: що це таке насправді
Йонний зв’язок – це потужна електростатична сила, яка з’єднує позитивно заряджені катіони з негативно зарядженними аніонами в кристалічних ґратках солей та оксидів. Уявіть океан іонів, де кожен позитивний шукає пару з негативним, створюючи міцну структуру, від якої залежать смак солі на язику чи блиск кварцу в руках. Цей зв’язок виникає, коли метал віддає електрон неметалу, перетворюючись на заряджених сусідів, що притягуються за законом Кулона.
У повсякденному житті ми постійно стикаємося з його плодами: кухонна сіль NaCl тримає форму кристалів, а вапно CaO стає основою для будівельних матеріалів. Різниця електронегативності між атомами – ключ до цього дива: якщо вона перевищує 1,7, повний перенос електронів неминучий. Йонний зв’язок робить речовини твердими, як скеля, і розчинними у воді, де іони танцюють вільно.
На відміну від ковалентного “спільного дому” електронів, тут панує жорстка ієрархія зарядів, що визначає все – від високих температур плавлення до електропровідності в розплавах.
Як утворюється йонний зв’язок: крок за кроком
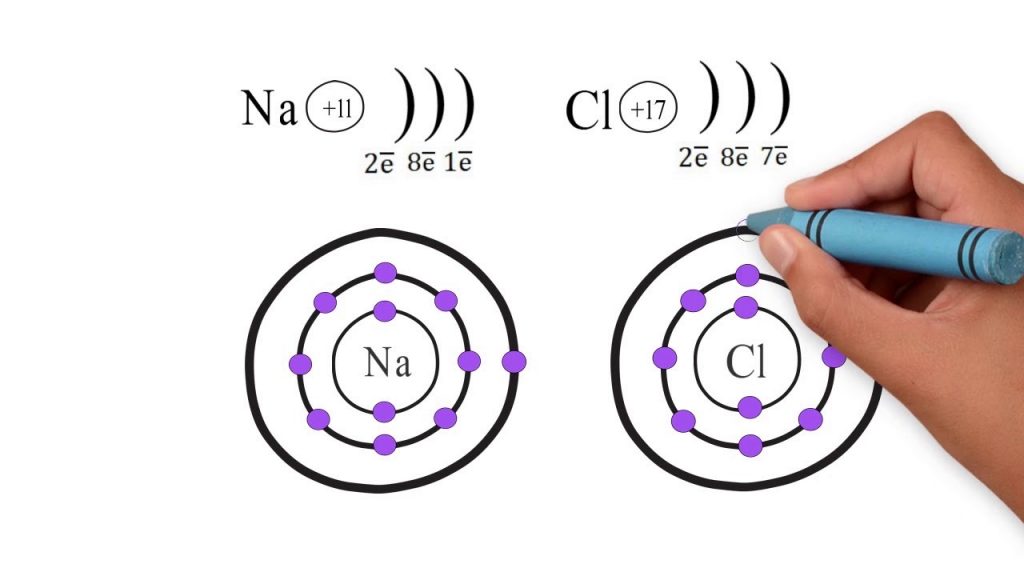
Атом натрію, з одним валентним електроном на зовнішній оболонці, легко віддає його хлору, який жадібно приймає пару для октету. Натрій перетворюється на Na⁺, хлор – на Cl⁻, і сили притягання зводять їх докупи в нейтральну сполуку NaCl. Цей процес енерговидільний: енергія сітки для NaCl сягає 787 кДж/моль, роблячи зв’язок неймовірно міцним.
У складніших випадках, як CaF₂, кальцій віддає два електрони двом фтору, утворюючи катіон Ca²⁺ і два аніони F⁻. Електронегативність грає роль диригента: метали лівої частини таблиці Менделєєва (низька ЕН) жертвують, неметали правої (висока ЕН) – хапають. Розгляньте рівняння:
- Na (атом) → Na⁺ + e⁻ (окиснення).
- Cl + e⁻ → Cl⁻ (відновлення).
- Na⁺ + Cl⁻ → NaCl (електростатичне притягання).
Після утворення іони не самотні – вони формують безкінечну ґратку, де кожен катіон оточений аніонами, ніби в оркестрі, де кожен грає свою партію. Така структура пояснює, чому йонні сполуки не мають окремих молекул, а є суцільним кристалом.
Приклади йонних сполук: від солі до перлин
Кухонна сіль NaCl – класика жанру, але є й екзотика: пероксид натрію Na₂O₂ для відбілювання, чи фторид кальцію CaF₂ у кришталі для оптики. Оксиди металів, як MgO в магнезії для шлунка чи антиперспірантів, демонструють універсальність. Гідроксиди, наприклад KOH у мильному виробництві, теж тримаються йонними силами.
Складні солі додають шарму: аміачна селітра NH₄NO₃ з йонами NH₄⁺ і NO₃⁻, де органічний катіон грає з неорганічним аніоном. Перед таблицею порівнянь ось ключові приклади:
- NaCl: повсякденна сіль, tпл 801°C.
- MgO: вогнетривкий матеріал, tпл 2825°C.
- CsCl: модель для великих катіонів, координаційне число 8.
- ZnS: сфалерит, напівпровідник у лампах.
Ці сполуки не просто формули – вони в їжі, медицині, електроніці, нагадуючи, як мікросвіт формує макроречі.
Фізичні властивості: чому йонні сполуки такі вперті
Йонні кристали тверді та крихкі, бо зміщення шарів іонів одного знаку призводить до відштовхування, ламаючи структуру. Високі температури плавлення – наслідок сильних кулонівських сил: для NaCl потрібно 801°C, для Al₂O₃ аж 2072°C. У розплавах чи розчинах вони проводять струм, бо іони рухаються вільно.
Розчинність залежить від енергії гідратації: NaCl чудово розчиняється у воді (359 г/л), а AgCl – ні, бо малі Ag⁺ слабо гідратуються. Щільність коливається: від 2 г/см³ для NaCl до 5 для PbS.
| Сполука | t плавлення, °C | t кипіння, °C | Енергія сітки, кДж/моль |
|---|---|---|---|
| NaCl | 801 | 1413 | 787 |
| MgO | 2825 | 3600 | 3791 |
| CaF₂ | 1418 | 2532 | 2600 |
| LiF | 845 | 1676 | 1030 |
Дані з uk.wikipedia.org та підручників хімії. Більші заряди чи менші відстані між іонами посилюють зв’язок, роблячи речовини стійкішими до спеки.
Кристалічні ґратки: архітектура іонів
У NaCl – гранецентрована кубічна ґратка, де кожен Na⁺ оточений 6 Cl⁻, як у рок-залі. CsCl має просту кубічну, з координацією 8:1, бо великий Cs⁺ вміщує більше сусідів. ZnS у сфалериті – цинк у тетраедрі сірки, впливаючи на напівпровідникові властивості.
Правило радіусних співвідношень Фаяльса визначає тип: для r⁺/r⁻ 0.414-0.732 – октаедрична координація, як у NaCl. Ці структури видно на рентгенограмах, розкриваючи таємниці блиску кристалів. Різноманітність пояснює, чому одні солі прозорі, інші – кольорові через дефекти.
Порівняння з іншими зв’язками: таблиця відмінностей
Йонний зв’язок контрастує з ковалентним і металічним, впливаючи на властивості. Ось структуроване порівняння для ясності:
| Характеристика | Йонний | Ковалентний | Металічний |
|---|---|---|---|
| Механізм | Перенос e⁻ | Спільна пара | Море delocalized e⁻ |
| t плавлення | Висока | Низька-молекулярні | Висока |
| Провідність | У розплавах/р-нах | Ізолятори | У твердому стані |
| Направленість | Немає | Є | Немає |
За даними khanacademy.org. Йонний – король солей, ковалентний – для газів, металічний – для провідників.
Цікаві факти про йонний зв’язок
- У надкритичних умовах NaCl стає металом – іони “тануть” у плазмі!
- Дефект Френкеля в AgCl робить його фотоемульсією для плівок.
- Іонні рідини – розплави солей при кімнатній t, революція для “зеленої” хімії 2020-х.
- У біології Na⁺/K⁺-насос у клітинах – йонний градієнт для життя.
- MgO витримує 3600°C – матеріал для космічних двигунів.
Ці перлини роблять хімію живою наукою, повною сюрпризів.
Сучасні застосування: від батарейок до нанотехнологій
Йонні сполуки в Li-ion батареях: Li⁺ мігрує між електродами, забезпечуючи енергію смартфонам. Суперконденсатори з іонними рідинами обіцяють блискавичну зарядку електрокарів. У медицині – контрольоване вивільнення ліків з іонних матриць.
Фториди як LiF у ядерних реакторах, перхлорати в твердопаливних ракетах. Навіть у харчовій промисловості: фосфати як емульгатори. Майбутнє – твердотільні акумулятори з йонними провідниками, безпечніші за рідкі. Тренди 2026: іонні рідини для CO₂-поглинання, борючись зі зміною клімату.
Йонний зв’язок еволюціонує: від простих солей до розумних матеріалів, що змінюють світ. Його сила в простоті притягання зарядів продовжує надихати винахідників, відкриваючи нові горизонти хімії.







