Нітрили: властивості, синтез, застосування
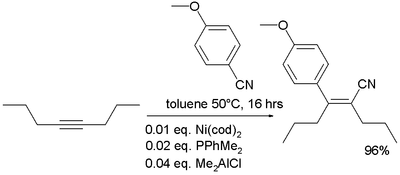
Що таке нітрили?
Нітрили – це клас органічних сполук, у яких центральною ланкою є нітрильна група (-C≡N), що складається з атома вуглецю, зв’язаного потрійним зв’язком із атомом азоту. Ці сполуки – наче хімічні чарівники: вони беруть участь у створенні пластмас, ліків і навіть космічних молекул, але водночас можуть бути небезпечними через свою токсичність. Нітрили є похідними ціановодню (HCN), де водень заміщений органічним радикалом, наприклад, метильною (CH₃) або фенільною (C₆H₅) групою.
Їхня універсальність вражає: від рідкого ацетонитрилу, який пахне фруктами й розчиняє майже все, до твердих ароматичних нітрилів, що використовуються в складних синтезах. Вони – не просто хімічні речовини, а ключ до багатьох технологій, які змінюють наше життя.
Будова та властивості нітрилів
Нітрили мають унікальну структуру, яка робить їх такими особливими в хімії. Давайте розберемося, що робить їх такими реакційноздатними та корисними.
Хімічна структура
У серці нітрилів – нітрильна група -C≡N. Потрійний зв’язок між вуглецем і азотом – один із найміцніших в органічній хімії, що забезпечує стабільність, але водночас робить вуглець електрофільним, тобто привабливим для нуклеофілів. Атом вуглецю має sp-гібридизацію, що створює лінійну геометрію з кутом 180°.
- Полярність: Азот, більш електронегативний за вуглець, “тягне” електрони до себе, створюючи частковий позитивний заряд на вуглеці. Це робить нітрили ідеальними для реакцій із нуклеофілами.
- Резонанс: Нітрили мають дві резонансні форми, де вільна пара електронів азоту може координуватися з металами, утворюючи комплекси.
- Спектроскопія: У інфрачервоних спектрах нітрили видають себе чіткою смугою поглинання в межах 2220–2260 см⁻¹, що відповідає вібраціям потрійного зв’язку.
Фізичні властивості
Фізичні характеристики нітрилів варіюються залежно від їхньої молекулярної маси та природи радикала. Ось як вони поводяться в реальному світі.
| Нітрил | Формула | Температура кипіння (°C) | Розчинність у воді |
|---|---|---|---|
| Ацетонитрил | CH₃CN | 81,6 | Повна |
| Пропіонітрил | C₂H₅CN | 97 | Часткова |
| Бензонітрил | C₆H₅CN | 191 | Нерозчинний |
- Агрегатний стан: Нижчі нітрили (до 4 атомів вуглецю) – рідини з легким солодкуватим запахом, тоді як вищі – тверді речовини.
- Токсичність: Усі нітрили отруйні, але менш небезпечні, ніж ціановодень. Наприклад, ацетонитрил може викликати подразнення при тривалому контакті.
- Розчинність: Полярність нітрильної групи забезпечує розчинність нижчих нітрилів у воді, але з подовженням вуглецевого ланцюга вона зменшується.
Номенклатура нітрилів
Назви нітрилів формуються за чіткими правилами, щоб уникнути плутанини в науковій і промисловій практиці. Ось як це працює.
- За IUPAC: Назва утворюється від вуглеводню, де вуглець нітрильної групи вважається першим. Наприклад, CH₃CN – етанонітрил, CH₃CH₂CN – пропанонітрил.
- Похідні кислот: Нітрили називають за карбоновими кислотами, замінюючи “-ова кислота” на “-нітрил”. Наприклад, CH₃CN – нітрил оцтової кислоти (ацетонитрил).
- Ціанозамісники: У складних молекулах нітрильну групу позначають як “ціано-”. Наприклад, NCCH₂COOH – ціанооцтова кислота.
Така різноманітність назв дозволяє легко ідентифікувати нітрили в різних контекстах, від лабораторій до заводів.
Методи синтезу нітрилів
Нітрили можна отримати кількома способами, кожен із яких має свої переваги та обмеження. Ось найпоширеніші методи, які використовуються в хімії.
- Нуклеофільне заміщення: Галогеналкани реагують із ціанідами (NaCN, KCN) за механізмом Sₙ2, утворюючи нітрили. Наприклад: R-X + CN⁻ → R-CN + X⁻.
- Дегідратація амідів: Первинні аміди (RCONH₂) втрачають воду під дією дегідратуючих агентів, таких як P₂O₅ або SOCl₂. Реакція: RCONH₂ → RCN + H₂O.
- Аммоноліз кислот: Карбонові кислоти реагують із аміаком при високих температурах (300–450°C) у присутності каталізаторів (Al₂O₃). Наприклад, оцтова кислота дає ацетонитрил.
- Окислювальна аммоноліз: Промисловий синтез акрілонітрилу відбувається шляхом окислення пропілену в присутності аміаку та кисню: 2CH₂=CHCH₃ + 2NH₃ + 3O₂ → 2CH₂=CHCN + 6H₂O.
Ці методи дозволяють отримувати нітрили в лабораторних і промислових масштабах із високою ефективністю.
Хімічні реакції нітрилів
Нітрили – це справжні хімічні “акробати”, які беруть участь у різноманітних реакціях завдяки електрофільності вуглецю в групі -C≡N. Ось ключові перетворення, які роблять їх незамінними.
Гідроліз
Нітрили гідролізуються до амідів, а потім до карбонових кислот у присутності кислот або лугів.
- Механізм: Нуклеофіл (H₂O або OH⁻) атакує вуглець, утворюючи проміжний гідроксиімін, який перетворюється на амід. Подальший гідроліз дає кислоту.
- Реакція: RCN → RCONH₂ → RCOOH (або RCOO⁻ у лужному середовищі).
- Умови: Кислотний гідроліз потребує сильних кислот (HCl, H₂SO₄), а лужний – NaOH або KOH.
Редукція
Нітрили можна відновити до первинних амінів за допомогою гідридів або каталітичного гідрування.
- Методи: Використовують LiAlH₄, NaBH₄ або H₂ із каталізатором (Ni, Pd).
- Реакція: RCN + 4H → RCH₂NH₂.
- Значення: Цей процес важливий для синтезу амінів, які є основою для ліків і барвників.
Реакція з реактивами Гріньяра
Нітрили реагують із магнійорганічними сполуками, утворюючи кетони після гідролізу.
- Механізм: Реактив Гріньяра (R’MgX) додається до вуглецю, формуючи імін, який гідролізується до кетону (RCOR’).
- Застосування: Використовується для синтезу складних органічних молекул.
Інші реакції
- Реакція Ріттера: Нітрили реагують із алкенами чи спиртами в кислотному середовищі, утворюючи заміщені аміди.
- Координація з металами: Нітрили утворюють комплекси з перехідними металами (Cu, Ni, Pd), що використовується в каталізі.
- Тіоаміди: Реакція з H₂S перетворює нітрили на тіоаміди (RC(S)NH₂).
Застосування нітрилів
Нітрили – це хімічні “робочі конячки”, які знаходять застосування в найрізноманітніших галузях. Ось де вони сяють.
- Розчинники: Ацетонитрил – улюбленець хіміків завдяки своїй здатності розчиняти органічні та неорганічні сполуки. Його використовують у хроматографії та синтезі.
- Полімери: Акрілонітрил – основа для виробництва поліакрілонітрильних волокон (одяг, килими) і пластмас, таких як ABS (корпуси техніки).
- Нітрильний каучук: Сополімери акрілонітрилу та бутадієну створюють стійкий до масел і палив каучук, який ідеально підходить для рукавичок, прокладок і шлангів.
- Фармацевтика: Нітрили є проміжними продуктами в синтезі антибіотиків, антидепресантів і протиракових препаратів.
- Медицина: Нітрильні рукавички, виготовлені з акрілонітрилу, популярні через їхню міцність і гіпоалергенність, особливо для людей із чутливістю до латексу.
Цікаві факти по темі: 🧬
Космічний слід: У 2008 році вчені виявили аміноацетонитрил у міжзоряній хмарі, що може бути ключем до розуміння походження життя!
Нітрильна міцність: Нітрильний каучук витримує розтягнення до 600%, що робить його незамінним у промислових виробах.
Історичний прорив: Перший синтез ацетонитрилу в XIX столітті відкрив двері до вивчення нітрилів як універсальних сполук.
Токсичність і безпека
Нітрили – це не лише корисні сполуки, а й потенційно небезпечні речовини, які вимагають обережності.
- Ризики: Вдихання парів або контакт із шкірою може викликати головний біль, нудоту чи подразнення. Акрілонітрил класифікується як можливий канцероген (група 2B за IARC).
- Захист: Працюючи з нітрилами, використовуйте захисні окуляри, рукавички та вентиляцію. Уникайте тривалого контакту.
- Екологія: Неправильна утилізація нітрилів може забруднити воду та ґрунт, тому промислові відходи обробляють із суворим контролем.
Нітрили – це хімічні супергерої, які творять дива в лабораторіях і на заводах, але вимагають поваги до їхньої сили. Їхня здатність бути одночасно корисними й небезпечними робить їх справжньою загадкою органічної хімії.
Джерело даних про хімічні властивості: McMurry J., Organic Chemistry, 9th Edition, Cengage Learning, 2016.