Скільки електронів може віддати атом магнію: глибинний огляд хімічних секретів
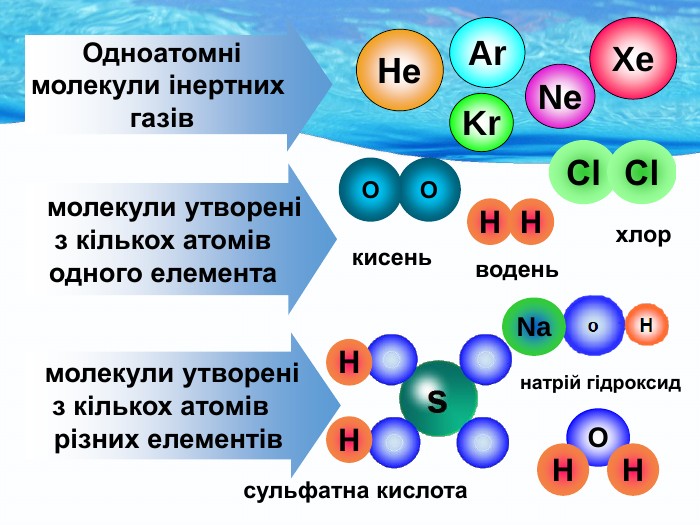
Атом магнію, цей непомітний герой періодичної таблиці, ховає в собі сили, що формують цілі галузі промисловості та біологічні процеси. З атомним номером 12, він стоїть у третьому періоді, у II групі, і його поведінка в реакціях нагадує впевненого дарувальника, що легко розлучається зі своїми скарбами. Коли ми говоримо про те, скільки електронів може віддати атом магнію, відповідь криється в його електронній оболонці – структурі, яка визначає, як цей елемент взаємодіє зі світом навколо. Цей метал не просто віддає електрони; він робить це з ентузіазмом, утворюючи сполуки, що підтримують життя на Землі, від зелених рослин до наших власних м’язів.
Уявіть магній як активного учасника хімічної вечірки: він завжди готовий поділитися своїми двома зовнішніми електронами, щоб досягти стабільності. Ця здатність робить його ключовим гравцем у реакціях окиснення-відновлення, де втрата електронів стає актом творення. Але давайте зануримося глибше, розбираючи цю тему крок за кроком, з акцентом на деталі, що часто губляться в загальних описах.
Електронна структура атома магнію: основа всього
Атом магнію складається з ядра з 12 протонами та, зазвичай, 12 нейтронами, оточеними хмарою з 12 електронів. Ці електрони не просто хаотично кружляють; вони організовані в шари, або енергетичні рівні, подібно до шарів цибулі, де кожен шар має свою роль. Перший рівень, найближчий до ядра, вміщує 2 електрони, другий – 8, а третій, зовнішній, – ще 2. Саме ці два зовнішні електрони роблять магній таким реактивним, адже вони прагнуть покинути атом, щоб досягти стабільної конфігурації, подібної до інертного газу неону.
Електронна формула магнію виглядає як 1s² 2s² 2p⁶ 3s². Тут ключ – у підрівні 3s²: ці два електрони на валентній оболонці визначають валентність елемента. У хімічних реакціях магній віддає саме їх, формуючи іон Mg²⁺. Це не випадковість; це результат позиції в періодичній системі, де елементи II групи, як-от берилій чи кальцій, поводяться схоже, віддаючи по два електрони. Якщо порівняти з натрієм, який віддає лише один, магній здається щедрішим, але це все через будову атома.
Детальніше розглядаючи, енергія іонізації – це кількість зусиль, потрібних для видалення електрона. Для магнію перша енергія іонізації становить близько 738 кДж/моль, а друга – 1450 кДж/моль, що робить втрату двох електронів можливим, але третій електрон відірвати вже надто складно, з енергією понад 7730 кДж/моль. Ось чому атом магнію в типових умовах віддає саме два електрони, не більше – це баланс між стабільністю та енергією.
Хімічні властивості магнію: чому він віддає саме два електрони
Магній – лужноземельний метал, сріблясто-білий і легкий, з густиною всього 1,74 г/см³, що робить його ідеальним для сплавів у авіації. Його хімічна активність проявляється в реакціях з киснем, водою чи кислотами, де він завжди втрачає два електрони. Наприклад, при горінні магнію в повітрі утворюється оксид MgO: 2Mg + O₂ → 2MgO. Тут кожен атом магнію віддає два електрони кисню, перетворюючись на іон з зарядом +2. Це не просто реакція; це демонстрація, як магній жертвує частинками себе для створення стабільних зв’язків.
У воді магній реагує повільніше, але з гарячою парою – бурхливо: Mg + H₂O → MgO + H₂. Знову ж, два електрони йдуть на утворення водню. А в кислотах, як соляна, Mg + 2HCl → MgCl₂ + H₂, магній формує солі з валентністю 2. Ці приклади підкреслюють, що в органічних і неорганічних сполуках магній рідко відходить від правила двох електронів. Винятки? У деяких комплексах, як хлорофіл, магній координується з чотирма азотами, але валентність залишається +2.
Фактор, що впливає, – ступінь окиснення. Для магнію він зазвичай +2, але в рідкісних випадках, як у субоксидах, може бути +1. Однак це нестабільні форми, і в стандартних умовах атом віддає два електрони. Згідно з даними з наукових джерел, таких як Вікіпедія, природний магній складається з ізотопів 24Mg (79%), 25Mg (10%) і 26Mg (11%), і всі вони поводяться однаково в плані електронів.
Практичні застосування: де магній демонструє свою щедрість
У промисловості магній використовують у сплавах, як AM60 для автомобільних деталей, де його здатність віддавати електрони забезпечує корозійну стійкість. У медицині магній – частина солей, як сульфат магнію, що розслаблює м’язи, бо іон Mg²⁺ впливає на нервові імпульси. А в біології? Магній – серце хлорофілу, де він координує фотони для фотосинтезу, віддаючи електрони в ланцюгах перенесення.
Ще один аспект – електрохімія. У магнієвих батарейках атом магнію на аноді віддає два електрони, генеруючи струм: Mg → Mg²⁺ + 2e⁻. Це робить його перспективним для екологічних джерел енергії, адже магній рясний і дешевий. Уявіть батареї, що працюють на морській воді, де магній реагує з киснем, виробляючи енергію без шкідливих викидів.
Але не все ідеально: магній горючий, і його спалахи використовують у феєрверках, де швидка втрата електронів створює яскраве світло. Це нагадує, як невелика деталь – два електрони – може призвести до грандіозних ефектів.
Роль магнію в біологічних процесах
У людському тілі магній бере участь у понад 300 ферментативних реакціях, завжди як Mg²⁺. Він стабілізує АТФ, молекулу енергії, віддаючи електрони для фосфорилювання. Брак магнію призводить до втоми, бо клітини не можуть ефективно переносити енергію. Дослідження показують, що дорослим потрібно 300-400 мг магнію на день, і він надходить з горіхів, шпинату чи бананів.
У рослинах магній – центр хлорофілу, де його іон поглинає світло, запускаючи електронний транспорт. Без цих двох електронів фотосинтез зупинився б, і планета втратила б кисень. Це робить магній не просто елементом, а основою життя.
Вплив на сучасні технології та екологію
У 2025 році магній набуває нового значення в зелених технологіях. У водневих паливних елементах магнієві гідриди зберігають водень, де магній віддає електрони для вивільнення газу. Це крок до чистої енергії, адже запаси магнію величезні – понад 2% земної кори.
Екологічно магній корисний у очищенні води: його сполуки осаджують забрудники, використовуючи валентність +2. Але видобуток магнію, часто з морської води, вимагає енергії, і вчені шукають сталі методи, як електроліз з відновлюваних джерел.
У космічних технологіях магнієві сплави легкі та міцні, допомагаючи ракетам долати гравітацію. Тут атом магнію, віддаючи електрони в сплавах, забезпечує стійкість до корозії в вакуумі.
Цікаві факти про магній
- 🔥 Магній горить білим полум’ям при 650°C, і його неможливо загасити водою – це через інтенсивну втрату електронів, що генерує тепло.
- 🌿 У хлорофілі магній заміняє залізо, роблячи рослини зеленими; без нього листя жовкло б, як у випадку дефіциту.
- 🚀 Магній відкрив Гемфрі Деві в 1808 році, назвавши на честь Магнезії, грецького регіону – історичний факт, що додає романтики елементу.
- 💊 Більше 50% магнію в тілі – в кістках, де він допомагає кальцію, формуючи міцну структуру через іонні зв’язки.
- ⚡ Магнієві аноди захищають кораблі від корозії, жертвуючи електронами замість заліза – справжній хімічний лицар.
Ці факти не просто курйози; вони ілюструють, як два електрони магнію впливають на світ. Уявіть, як цей елемент, віддаючи частинку себе, формує реальність від мікроскопічних клітин до космічних польотів.
Потенціал і обмеження: чи може магній віддати більше?
Теоретично, під екстремальними умовами, як у плазмі чи при високих тисках, магній міг би втратити більше електронів, але в реальності це не відбувається. Дослідження в лабораторіях, наприклад, з лазерним випаровуванням, показують, що третій електрон вимагає енергії, еквівалентної зірковим температурам. Тому в хімії ми говоримо про два – це консенсус з джерел, як журнал Nature.
У квантовій механіці орбіталі магнію пояснюють цю межу: після втрати 3s² атом досягає стабільної конфігурації [Ne], і подальша іонізація руйнує цю гармонію. Це робить магній передбачуваним, але й обмеженим у порівнянні з перехідними металами, як залізо, що змінює валентність.
Для студентів і ентузіастів: експериментуйте з магнієвою стрічкою в кислоті, спостерігаючи бульбашки водню – прямий доказ двох електронів у дії. Але будьте обережні, бо реакція гаряча!
| Аспект | Деталі | Приклад |
|---|---|---|
| Електронна конфігурація | 1s² 2s² 2p⁶ 3s² | Зовнішні 2 електрони на 3s |
| Валентність | Зазвичай +2 | MgO, MgCl₂ |
| Енергія іонізації | 1-а: 738 кДж/моль; 2-а: 1450 кДж/моль | Легко втрачає 2, важко 3 |
| Застосування | Сплави, медицина, енергія | Батарейки, хлорофіл |
Ця таблиця підсумовує ключові моменти, базуючись на даних з джерел як Вікіпедія та Pharmencyclopedia. Вона показує, чому магній – ідеальний дарувальник двох електронів, балансуючи між активністю та стабільністю.
Розглядаючи майбутнє, у 2025 році дослідження фокусуються на наноматеріалах з магнієм, де контроль над електронами може призвести до суперконденсаторів. Це нагадує, як простий атом, віддаючи всього два електрони, продовжує дивувати науковців і змінювати світ.